乙酸鈉

|
|

|
|

|
|
| 名稱 | |
|---|---|
|
首選IUPAC名稱
乙酸鈉 |
|
| 其他名稱
熱冰(醋酸鈉三水合物)
|
|
| 身份標識 | |
|
3D模型( JSMOL )
|
|
| 3595639 | |
| 切比 |
|
| chembl |
|
| Chemspider |
|
| 藥品銀行 |
|
| echa inforcard | 100.004.386 |
| EC編號 |
|
| E號碼 | E262 (防腐劑) |
| 20502 | |
| kegg |
|
|
PubChem CID
|
|
| RTECS編號 |
|
| unii |
|
|
COMPTOX儀表板( EPA )
|
|
|
|
|
|
| 特性 | |
| C 2 H 3 Na O 2 | |
| 摩爾質量 | 82.034 g·mol -1 |
| 外貌 | 白色派粉 |
| 氣味 | 加熱到分解時醋(乙酸)氣味 |
| 密度 | 1.528 g/cm 3 (20°C,無水) 1.45 g/cm 3 (20°C,三水合物) |
| 熔點 | 324°C(615°F; 597 K) (無水) 58°C(136°F; 331 K) (三水合物) |
| 沸點 | 881.4°C(1,618.5°F; 1,154.5 K) (無水) 122°C(252°F; 395 K) (三水合)分解 |
| 無水: 119 g/100 mL(0°C) 123.3 g/100 mL(20°C) 125.5 g/100 mL(30°C) 137.2 g/100 mL(60°C) 162.9 g/100 mL(100°C) 三水合物: 32.9 g/100 mL(-10°C) 36.2 g/100 mL(0°C) 46.4 g/100 mL(20°C) 82 g/100 mL(50°C) |
|
| 溶解度 | 可溶於酒精,肼,所以2 |
| 甲醇中的溶解度 | 16 g/100 g(15°C) 16.55 g/100 g(67.7°C) |
| 乙醇中的溶解度 | 三水合物: 5.3 g/100毫升 |
| 丙酮中的溶解度 | 0.5 g/kg(15°C) |
| 酸度(P K A ) | 24(20°C) 4.75(與CH 3 COOH混合為緩衝液時) |
| 基礎性(P K B ) | 9.25 |
|
磁化率 (χ)
|
-37.6·10 -6 cm 3 /mol |
|
折射率( N D )
|
1.464 |
| 結構 | |
| 單斜利 | |
| 熱化學 | |
|
熱容量( C )
|
100.83 J/mol·K(無水) 229 J/mol·K(三水合物) |
|
STD磨牙
熵( S⦵298 ) |
138.1 J/mol·K(無水) 262 J/mol·K(三水合物) |
|
STD焓
形成( δFH⦵298 ) _ |
-709.32 kJ/mol(無水) -1604 kJ/mol(三水合物) |
|
吉布斯自由能( δf g⦵ )
|
-607.7 kJ/mol(無水) |
| 藥理 | |
| B05XA08 ( WHO ) | |
| 危險 | |
| 職業安全與健康(OHS/OSH): | |
|
主要危害
|
刺激性 |
| NFPA 704 (消防鑽石) | |
| 閃點 | > 250°C(482°F; 523 K) |
| 600°C(1,112°F; 873 K) | |
| 致命劑量或濃度(LD,LC): | |
|
LD 50 (中位劑量)
|
3530 mg/kg(口腔,大鼠) |
| 安全數據表(SD) | 外部MSD |
| 相關化合物 | |
|
其他陰離子
|
甲酸鈉 丙酸鈉 |
|
其他陽離子
|
乙酸鉀 乙酸鈣 |
|
相關化合物
|
二乙酸鈉 |
|
除非另有說明,否則給出了其標準狀態(25°C [77°F],100 kPa)的材料的數據。
Infobox參考
|
|
乙酸鈉,Ch 3 Coona,也縮寫為Na O AC ,是乙酸的鈉鹽。這種無色的二線鹽具有廣泛的用途。
申請
生物技術
乙酸鈉用作培養細菌的碳源。乙酸鈉也可用於通過乙醇沉澱增加DNA分離的產量。
工業的
乙酸鈉用於紡織工業中,用苯胺染料中和硫酸廢料流中和光劑。它也是鍍鉻曬黑中的醃製劑,有助於阻礙合成橡膠生產中氯普倫的硫酸鹽。在處理一次性棉墊的棉花時,乙酸鈉用於消除靜電的積累。
具體的壽命
乙酸鈉用於通過充當混凝土密封劑來減輕對混凝土的損害,同時也比常用的環氧樹脂替代方案在環境上良性且便宜,用於將混凝土封閉於水滲透。
食物
乙酸鈉可以作為調味料添加到食物中,有時以二乙酸鈉的形式,二乙酸鈉,乙酸鈉和乙酸的一對一絡合物,鑑於E-Number E262 。它通常用於給薯片呈鹽和醋味,可以用作薯片上醋本身的替代品,因為它不會為最終產品添加水分。乙酸鈉(無水)被廣泛用作保質期擴展劑和pH控製劑。低濃度的食物是安全的。
緩衝溶液
乙酸鈉(乙酸的鹼性鹽)和乙酸的溶液可以作為緩衝液保持相對恆定的pH水平。這在反應依賴於在溫和酸性範圍內的pH值(pH 4-6)的生化應用中尤其有用。
加熱墊

乙酸鈉還用於加熱墊,手動加熱器和熱冰中。乙酸鈉在水中的過飽和溶液提供了一種啟動結晶的裝置,該工藝釋放了大量熱量。

乙酸鈉三水合物晶體在58-58.4°C(136.4–137.1°F)處融化,溶解在其結晶水中。當它們通過熔點加熱並隨後使它們冷卻時,水溶液變得過飽和。該溶液能夠冷卻至室溫,而無需形成晶體。通過按加熱墊中的金屬盤,形成了成核中心,從而導致溶液將其結晶回乙酸鈉三水合物中。結晶過程是放熱的。融合的潛熱約為264-289 kJ/kg。與某些類型的熱包(例如依賴不可逆的化學反應的熱包)不同,乙酸鈉熱包可以通過將包裝浸入沸水中幾分鐘來輕鬆重複使用,直到晶體完全溶解,並使包裝緩慢緩慢地溶解冷卻到室溫。
準備

為了實驗室使用,乙酸鈉價格便宜,通常購買而不是合成。它有時是在實驗室實驗中通過乙酸的反應而產生的,乙酸的反應通常是在5-8%的溶液中,稱為醋,碳酸鈉(“洗蘇打水”),碳酸氫鈉(“小蘇打”)或氫氧化鈉( “鹼液”或“苛性蘇打”)。這些反應中的任何一種產生乙酸鈉和水。當將含鈉和碳離子化合物用作反應物時,來自碳酸氫鈉或碳酸鈉的碳酸鹽陰離子與乙酸中的羧基(-cooH)中的氫反應,形成碳酸。碳酸在正常條件下易於分解成氣態的二氧化碳和水。這是在著名的“火山”中發生的反應,當將家用產品(小蘇打和醋)合併時。
- CH 3 COOH + NAHCO 3 →CH 3 COONA + H 2 CO
3 -
H 2 Co
3 → CO
2 + h
2 o
從工業上講,乙酸鈉三水合物是通過使用水作為溶劑與氫氧化鈉反應來製備的。
- CH 3 COOH + NAOH→CH 3 COONA + H 2O 。
為了在工業上生產無水醋酸鈉,使用了煙液過程。將鈉金屬嵌入鈉通過模具擠出,形成鈉金屬的帶,通常在惰性氣氣中,例如n 2 ,然後浸入無水乙酸中。
- 2 CH 3 COOH + 2 Na→2 Ch 3 Coona + H 2 。
氫氣通常是有價值的副產品。
結構
無水醋酸鈉的晶體結構已被描述為交替的羧酸鈉和甲基層。乙酸鈉三水合物的結構由鈉的八面體配位組成。鄰近的八面體共享邊緣形成一維鏈。在乙酸離子和水合水之間的兩個維度的氫鍵將鏈連接到三維網絡。
| 水合程度 | 無水 | 三水合物 |
|---|---|---|
| NA協調 |
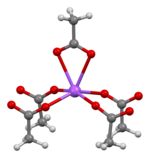
|

|
| 牢固的聚集 |
 2D紙 |
 1D鏈 |
| 較弱的粘合聚集 |
 床單堆疊在一起 接觸中的疏水錶面 |
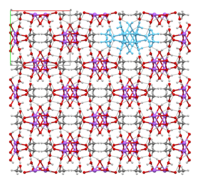 由氫鍵連接的鏈 (淺藍色突出顯示的一條鏈) |
反應
- CH 3 Coona + BRCH 2 CH 3 → CH 3 COOCH 2 CH 3 + NABR
乙酸鈉在強迫條件下(氫氧化鈉)在強迫條件下經歷脫羧(CH 4 ):
- CH 3 Coona + NaOH→CH 4 + NA 2 CO 3
氧化鈣是用於該反應的典型催化劑。剖腹鹽也催化了這一反應。
